Боль в груди и одышка у взрослых — две наиболее распространенные причины обращения за медицинской помощью к специалистам амбулаторного звена и вызова скорой помощи. Эта глава посвящена лабораторным методам, используемым в дифференциальной диагностике этих симптомов. К этим тестам относится измерение уровня в сыворотке / плазме крови тропонинов (ТнТ и Тн1), и креатин(фосфо)киназы (МВ-КФК) и мозгового натрийуретического пептида. Хотя перечисленные соединения никак не связаны между собой (ни структурно, ни функционально), все они входят в состав кардиомиоцитов и высвобождаются в кровь при повреждении миокарда. Поэтому их называют сердечными (сердечно-сосудистыми, миокардиальными) маркерами. Основное назначение первых двух тестов (тропонина и КК) — помочь выявить пациентов, у которых боль в груди появляется вследствие инфаркта миокарда — острого жизнеугрожающего проявления заболеваний сердца, часто называемого сердечным приступом.
Ежегодно в Великобритании острый инфаркт миокарда переносят около 125 000 человек. Повреждение сердечной мышцы бывает настолько тяжелым, что может вызвать молниеносные летальные аритмии, остановку сердца и внезапную сердечную смерть; около 20% больных умирают до оказания медицинской помощи. Ранняя диагностика и своевременное лечение могут спасти жизнь выживших пациентов и минимизировать существующую для сердца опасность. Так, в настоящее время выживают около 90% пациентов, доставленных в госпитали с инфарктом миокарда.
Основное назначение третьего теста, сывороточного BNP, — диагностика сердечной недостаточности (СН), ранним симптомом которой служит одышка, возникающая после минимальной нагрузки. Сердечная недостаточность — это хроническое прогрессирующее состояние, причиной которого может стать инфаркт миокарда и длительная гипертензия. В Великобритании сердечной недостаточностью страдают около 900 000 человек. Это болезнь пожилого возраста. Диагноз в большинстве случаев ставят лицам старше 65 лет. Заболеваемость наиболее высока среди очень пожилых людей (старше 84 лет). В этой возрастной группе сердечной недостаточностью страдает каждый десятый.
Тропонин
В организме человека три основных типа мышц: гладкая мускулатура стенки полых органов, функционирование которых зависит от сокращения их стенки (желудочно-кишечный тракт, мочевой пузырь, кровеносные сосуды и т. д.); скелетная мускулатура и сердечная мышца (миокард), которая составляет основную массу сердца.
Белок тропонин (Тн) входит в состав миоцитов сердечной и скелетных мышц как структурный компонент сократительной системы, которая обеспечивает мышечное сокращение. Он состоит из трех полипептидных субъединиц — тропони- на С (ТнС), тропонина I (Тн!) и тропонина Т (ТнТ). Тропони- новый комплекс локализуется в актиновых филаментах мио- фибрилл. Взаимодействие между актиновыми и миозиновы- ми филаментами, лежащее в основе мышечного сокращения, инициируется ионами кальция, связанными с тропонином С. Ингибирует сокращение связывание актина с тропонином I. Таким образом, тропонин, участвуя в двух разнонаправленных процессах (запуск и прекращение сократительной реакции), играет важную роль в регуляции сокращения сердечной и скелетных мышц.
Существуют тканеспецифичные изоформы тропонинов С, I и Т. Это означает, что между тропонинами сердца (сТн) и тропонинами скелетных мышц существуют различия. В норме тропонин содержится в миоцитах скелетных мышц и кардиомиоцитах, а в крови практически не определяется. Но при повреждении мышечной ткани содержимое миоцитов, в том числе тропонин, высвобождается в кровоток, поэтому содержание тропонина в плазме растет. Если поражается только миокард, то в крови повышается концентрация лишь специфических для сердца изоформ тропонина — сТнС, сТнI и сТнТ.
Для оценки состояния больных с грудной болью используют 2 основных теста определения тропонина. В некоторых лабораториях в этих случаях измеряют концентрацию сТнТ в сыворотке/плазме, в других предпочитают определять содержание сТнI. Именно эти показатели были выбраны из множества других, так как они оказались наиболее чувствительными и специфичными для поражений сердца.
Креатинкиназа (МВ-КФК)
Креатинкиназа (другое название креатинфосфокиназа) — фермент, который катализирует перенос фосфата с креатинфосфата на аденозиндифосфат. Продуктами реакции являются креатин и макроэргическое соединение аденозинтрифосфат:
креатинфосфат + аденозиндифосфат → креатин + аденозинтрифосфат.
Креатинкиназа присутствует во многих типах тканей, но наибольшее количество определяется в сердечной мышце (миокарде), скелетных мышцах и в мозге.
Она состоит из двух белковых субъединиц, М и В, что позволяет идентифицировать три функционально одинаковых, но структурно различных изофермента КФК — ММ, ВВ и МВ. При определении уровня КФК в плазме получают суммарную активность всех трех изоферментов, но можно определить и активность каждого изофермента в отдельности. Креатинкиназа органоспецифична. Большая часть ВВ-КФК находится в мозге. В скелетных мышцах КФК представлена в основном изоферментом ММ, а в сердечной мышце — изоферментом МВ. Таким образом, МВ-КФК — это фракция креактинкина- зы, распространение которой ограничено исключительно кардиомиоцитами. В норме в крови содержится очень немного МВ-КФК, но при повреждении миокарда уровень этой фракции в плазме возрастает. МВ-КФК рассматривают как альтернативный сердечный маркер, если нет возможности определить содержание тропонина в крови.
Мозговой натрийуретический пептид (BNP)
Пептидами называются вещества, которые образованы простой цепью аминокислот (обычно менее 50). Мозговой натрийуретический пептид был впервые выделен из мозга свиней (отсюда его название), но у человека он синтезируется преимущественно в сердце, в частности в миоцитах — клетках, которые образуют мышечную стенку желудочков сердца. Родственное вещество, предсердный натрийуретический пептид (ANP) синтезируется в миоцитах, которые образуют стенки обоих предсердий. Все натрийуретические пептиды (существует еще два типа, которые не синтезируются в сердце) — это гормоны, участвующие в регуляции количества натрия и воды в крови и тем самым в регуляции объема крови, кровяного давления, а в конечном счете — функции сердца. Механизм действия и эффекты этих гормонов разнообразны, но наиболее важно то, что через ренин-ангиотензиновую систему они способствуют выведению натрия с мочой (натрийурез); это и нашло отражение в их общем названии.
Физиологическим стимулом для синтеза и секреции BNP в кровь служит растяжение желудочков, когда сердце работает интенсивнее, чем в нормальных условиях (например, при физических упражнениях). Миоциты желудочков синтезируют не сам BNP, а его предшественник про-BNP, состоящий из 108 аминокислот. В процессе секреции он расщепляется на два вещества, которые и поступают в кровь. Первое из них — это физиологически активный гормон BNP, состоящий из 32 аминокислот, а второе — физиологически неактивный пептид N-терминальный про-BNP (NT про-BNP), состоящий из 76 аминокислот. В некоторых лабораториях определяют концентрацию BNP, в других NT про-BNP. Для клинических целей оба анализа равноценны, но поскольку каждый из пептидов метаболизируется с разной скоростью, для каждого анализа существуют свои референтные (нормальные) значения.
Лабораторное измерение уровней тропонинов (сТнТ, сТнI) И МВ-КФК
Специальной подготовки не требуется.
Время взятия крови
В большинстве больниц разработан протокол, определяющий время сбора образцов крови для выявления сердечных маркеров у пациентов с болью в груди. Обычно кровь забирают при поступлении больного в стационар и повторно через 6-12 ч. Может понадобиться и выполнение анализа через 24 ч. Интерпретация результатов этих тестов во многом зависит от знания того, сколько времени прошло между взятием крови на анализ и моментом появления болей в груди. По этой причине очень важно на бланке анализа писать время взятия крови, время появления симптоматики (если оно известно) или время поступления пациента в больницу.
Количество крови и тип пробы
Для определения сердечных маркеров достаточно 5 мл крови. В принципе, эти маркеры можно определять как в сыворотке, так и в плазме крови, хотя уровень сТнТ удобнее измерять в сыворотке. Если в данной больнице принято использовать плазму, то кровь собирают в пробирки с антикоагулянтом (литиевой солью гепарина). Если в больнице работают преимущественно с сывороткой, то кровь собирают в обычные пробирки без каких-либо добавок. Гемолизированные пробы не годятся для определения уровня тропонина; в этом случае кровь необходимо взять повторно.
Интерпретация результатов
Референтные значения
Однозначно определить референтные значения для этих показателей невозможно, так как они сильно варьируют и зависят от принятой в лаборатории методологии. Поэтому интерпретация результатов анализа должна опираться на полученные в данной лаборатории референтные значения и принятые диагностические критерии. Достаточно вспомнить, что у здоровых людей сердечные маркеры в крови находятся в очень незначительных количествах (а часто вообще не определяются).
По последним рекомендациям, единицей для измерения ТнI и Т служит нанограмм в литре (нг/л), но в некоторых лабораториях продолжают пользоваться единицами нг/мл или мг/л. Чтобы перевести результат из старых единиц в новые, нужно умножить его на 1000.
Причины повышения уровня в сыворотке / плазме тропонинов и креатинкиназы
Единственная причина роста концентраций сТнТ и сТн1 в сыворотке / плазме крови — это гибель кардиомиоцитов (некроз миокарда). По этой же причине (но не только) происходит увеличение таких показателей, как сывороточный (плазменный) миоглобин и МВ-КФК. Наиболее вероятная причина некроза миокарда — инфаркт.
Инфаркт миокарда и ишемическая болезнь сердца
Всем живым клеткам необходима постоянная доставка оксигенированной крови. Ишемия — термин, используемый для описания неадекватной доставки кислорода к какому-либо участку ткани, а под инфарктом подразумевается гибель ткани в результате тяжелой или длительной ишемии. Инфаркт миокарда — это гибель кардиомиоцитов в ишемизированной области миокарда. Практически в случае развития инфаркта миокарда ишемия развивается в рамках ишемической болезни сердца (ИБС).
Атеросклеротическая бляшка — патофизиологическое повреждение, лежащее в основе развития ИБС. Атеросклероз представляет собой образование локальных скоплений жировых отложений и фрагментов клеток, покрытых фиброзной оболочкой, на внутренней поверхности артерий (в том числе коронарных). После длительного (много лет) латентного периода бляшка может вырасти до размеров, существенно ограничивающих кровоток — настолько, что у больного начинают появляться характерные симптомы, свидетельствующие об ограничении доставки кислорода к сердечной мышце. Главный из них — боль в груди, которая ощущается скорее как некий дискомфорт, а не как острая или режущая боль. Обычно ишемическую боль описывают как стесняющую грудную клетку, давящую, сжимающую, душащую. Как правило, она поражает область грудной клетки диффузно и может иррадии- ровать в шею, горло, челюсть, плечо, руку. Наименее тяжелое и самое распространенное проявление ИБС — это ишемические боли в груди, ассоциирующиеся со стабильной стенокардией. У таких больных боль или дискомфорт в груди появляется в момент увеличения потребности сердца в кислороде, например, во время физического напряжения или эмоционального стресса, что вызывает увеличение частоты сердечных сокращений (ЧСС). Неприятные симптомы проходят при расслаблении, как только уменьшается потребность сердца в кислороде. При стабильной стенокардии уменьшение доставки кислорода к миокарду вызывает боль в груди, недостаточную для гибели кардиомиоцитов. Следовательно, у таких больных уровень сердечных маркеров в сыворотке / плазме не увеличивается.
Иногда первым проявлением ИБС оказывается не стабильная стенокардия, а более опасный острый коронарный синдром (ОКС). Под этим названием подразумевается не одно заболевание, а целый ряд болезней нарастающей тяжести, включая инфаркт миокарда. Патогенетической основой ОКС служат нестабильные атеросклеротические бляшки.
По непонятным до конца причинам покрывающая атеросклеротическую бляшку с ее содержимым (липиды, клеточный материал) фиброзная оболочка («шапочка») может истончаться, становиться хрупкой и разрываться. Пациенты с нестабильными атеросклеротическими бляшками имеют наиболее высокий риск развития жизнеугрожающих осложнений ИБС. К разорвавшейся бляшке, содержимое которой представляет собой потенциальный субстрат для запуска реакций свертывания крови, мигрируют тромбоциты. Тромб, образовавшийся на месте разрыва бляшки, может частично или полностью перекрыть кровоток в данном сосуде. Кроме того, остатки клеток, освободившиеся из бляшки, и фрагменты тромба могут закупоривать более мелкие сосуды в местах, удаленных от первоначального места нахождения бляшки. Это и определяет разнообразие клинических симптомов, связанных с повреждением атеросклеротических бляшек, которые наблюдаются при ОКС.
Наиболее безопасное проявление ОКС — это нестабильная стенокардия. Для нее, как и для стабильной стенокардии, характерна та же боль в груди (или дискомфорт). Но при нестабильной стенокардии боль появляется и в покое или при незначительной нагрузке, имеет более выраженную интенсивность и более продолжительна. Важной чертой нестабильной стенокардии, единственно отличающей ее от инфаркта миокарда (более опасное проявление ОКС), служит отсутствие некротических изменений в миокарде. Значит, при нестабильной стенокардии не наблюдаются и патологические изменения в уровнях сердечных маркеров. Но поскольку нестабильная стенокардия связана с наличием нестабильных атеросклеротических бляшек в коронарных артериях, у больных существенно повышен риск развития инфаркта миокарда в ближайшем будущем. Примерно у 15% пациентов через неделю после постановки диагноза нестабильной стенокардии случается инфаркт миокарда.
Инфаркт миокарда и сердечные маркеры
Если ишемия, возникшая в результате окклюзии артерии, в том числе тромбом, выраженная и длительная, кардиомиоциты, кровоснабжаемые ею, погибают. Это и есть инфаркт миокарда. Масса инфарцированного миокарда варьирует в широких пределах (от < 1 до > 25 г) в зависимости от места окклюзии, что отражается разными изменениями на ЭКГ и величиной смертности. Во всех случаях повышаются уровни сердечных маркеров в сыворотке / плазме. Обязательный диагностический критерий инфаркта миокарда — увеличение содержания тропонина (сТнТ и сТн1) или активности МВ-КФК. Степень такого повышения отражает объем поражения, а значит, тяжесть инфаркта.
В большинстве случаев сильная давящая боль (или дискомфорт) в груди в покое, продолжающаяся не менее 20 мин, означает начало тяжелого инфаркта миокарда. Дополнительные симптомы включают затрудненное дыхание, легкое головокружение, потливость, тошноту и рвоту. Углубление ишемии отражается на ЭКГ изменениями (подъем сегмента ST), которые дали название тяжелому варианту инфаркта — инфаркт с элевацией (подъемом) сегмента ST (ИМ-ST). Некроз кардиомиоцитов начинается не сразу, а через 10-15 мин после начала ишемии. Он увеличивает риск для больного постепенно, в течение следующих 4-6 ч, что дает возможность осуществить лечебное воздействие (тромболитическая терапия / реперфузия) для ограничения поражения сердца.
Рост уровня сердечных маркеров в плазме после инфаркта миокарда — преходящее явление, связанное со временем наступления инфаркта. В первый час после появления симптоматики никаких изменений не наблюдается.
Рост уровней сТнТ, сТн1 и МВ-КФК, как правило, начинается в диапазоне 3-6 ч после появления симптомов, хотя в ряде случаев это происходит раньше. Пик концентрации достигается примерно через 12-24 ч после инфаркта.
Уровень МВ-КФК обычно уже через 2-3 дня возвращается к норме, но концентрация тропонинов сохраняется повышенной значительно дольше — иногда свыше двух недель после инфаркта.
Диагноз инфаркта миокарда, как правило, исключают как причину боль в груди, если уровни МВ-КФК или тропонинов остаются в нормальных пределах в течение 12 ч после обнаружения симптомов болезни. При наличии сомнений целесообразно повторить тестирование через сутки. Если результат снова оказывается нормальным, диагноз инфаркта можно однозначно исключить. Однако это не исключает того, что боль в груди имеет кардиальное происхождение, так как у больных со стенокардией (стабильной и нестабильной) уровни сердечных маркеров не повышены.
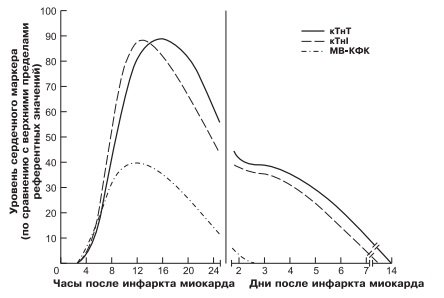
Типичные изменения уровней сердечных маркеров в разные сроки после инфаркта миокарда
Другие причины некроза миокарда
Хотя ишемия, ассоциирующаяся с инфарктом миокарда, — наиболее частая причина некроза миокарда, есть и другие причины, которые приводят к росту уровня сердечных маркеров. К ним относятся миокардит (инфекционное воспаление миокарда), перикардит (воспаление оболочек сердца), эмболия легочной артерии, травма сердца (например, при хирургическом вмешательстве) и сепсис. Обычно в этих условиях повышение уровней сердечных маркеров незначительное.
Лабораторное определение BNP
Специальной подготовки не требуется.
Время взятия крови
Кровь можно брать в любое время.
Количество крови и тип пробы
Достаточно 5 мл крови. Вид контейнера зависит от того, какой именно пептид определяют в данной лаборатории. Если в лаборатории определяют концентрацию BNP в плазме, то кровь берут в пробирку с антикоагулянтом ЭДТА; если определяют концентрацию NT про-BNP в сыворотке, то антикоагулянт не нужен, и кровь берут в простую пробирку.
Интерпретация результатов
Референтные значения для взрослых:
BNP в плазме — 10-150 пг/мл;
NT про-BNP в сыворотке — 80-250 пг/мл.
У женщин нормальные значения выше, чем у мужчин. У лиц обоего пола эти показатели значительно увеличиваются с возрастом. Так, у мужчин моложе 60 лет результаты будут около нижней границы нормальных значений, у женщин старше 80 лет — около верхней.
Анализ BNP и NT про-BNP при сердечной недостаточности
Концентрации BNP и NT про-BNP увеличиваются при некоторых сердечных и других заболеваниях (инфаркт миокарда, миокардит, почечная недостаточность, легочная гипертензия), но в настоящее время их анализ проводят только для диагностики сердечной недостаточности (СН).
Патогенез сердечной недостаточности сложен. Это хроническое прогрессирующее состояние, при котором сердце постепенно утрачивает способность перекачивать кровь в объеме, удовлетворяющем потребности организма. Основными причинами развития сердечной недостаточности служат инфаркт миокарда и хроническая гипертензия. Из-за недостаточного кровообращения ткани получают мало кислорода, что проявляется такими симптомами, как быстрая утомляемость, головокружение, слабость. Существуют компенсаторные механизмы, которые помогают в течение короткого времени, но неизбежно приводят к возрастанию нагрузки на сердце и поэтому усугубляют сердечную недостаточность. Один из этих механизмов — задержка жидкости, чтобы увеличить объем крови. Это приводит к развитию периферических отеков и застою в легких. Характерные симптомы СН — отечные, болезненные лодыжки, а также одышка, которая возникает при самом незначительном напряжении, а при прогрессировании СН и в покое.
Еще один компенсаторный механизм — изменение размеров сердца. Оно увеличивается, желудочки растягиваются. В результате растяжения стенок желудочков в миоцитах, из которых они состоят, увеличивается продукция BNP и NT про-BNP.
Так как существуют другие состояние, приводящие к увеличению концентрации BNP и NT про-BNP, этот тест нельзя использовать для точной диагностики СН. Наиболее надежно СН выявляют с помощью эхокардиографии, неинвазивного метода, который позволяет получить изображение работающего сердца в реальном времени с помощью ультразвука. Концентрацию BNP и NT про-BNP определяют, чтобы исключить СН у лиц с жалобами на одышку, слабость и т. п. Если у таких пациентов результаты анализа BNP и NT про-BNP отрицательны, то СН маловероятна и нет необходимости в проведении эхокардиографии. В последних клинических руководствах эксперты рекомендуют использовать тесты на BNP и NT про-BNP и приводят данные для правильной интерпретации их результатов. В инструкциях Национального института здоровья и клинических стандартов сказано, что анализ BNP и NT про-BNP должен быть тестом первой линии в диагностическом процессе, если у пациента заподозрена СН, а в анамнезе у него нет инфаркта. Только те лица, у которых BNP больше 100 пг/мл или NT про-BNP больше 400 пг/мл нуждаются в эхокардиографии. У лиц с очень высокими показателями (BNP > 400 пг/мл или NT про-BNP > 2000 пг/мл) прогноз плохой, они нуждаются в срочной эхокардиографии (в течение двух недель).
Tак как концентрация BNP/NT про-BNP соответствует тяжести СН, эти тесты можно было бы использовать для мониторинга лечения. Диагностическое значение BNP и NT про-BNP уже признано, однако возможность их использования для мониторинга СН еще обсуждается.
Если в анамнезе нет инфаркта миокарда, только те лица, у которых «СН нельзя исключить» и «СН весьма вероятна», подлежат эхокардиографии. Лица с заключением «СН весьма вероятна» должны пройти это обследование в течение 2 недель. Пациенты с инфарктом миокарда в анамнезе и симптомами, подозрительными на СН, подлежат срочной эхокардиографии независимо от результатов теста на BNP/ NT про-BNP.