Прогноз рака желудка после того, как он вторгся в мышцы, является мрачным. В Соединенных Штатах на этой стадии диагностируется примерно две трети случаев, а общая 5-летняя выживаемость составляет 24% (Jemal et al., 2007). В Японии, стране с одним из самых высоких показателей заболеваемости раком желудка, поиск «ранних» раковых заболеваний является интенсивным. С 1960 года проводится массовая скрининговая программа. В категорию «ранний рак желудка» входят первичные опухоли, присутствующие в слизистой оболочке или подслизистой, но не в мышечной ткани. Иногда они метастазируют в соседние лимфатические узлы. Ранние карциномы все чаще обнаруживаются в Японии, в некоторых сериях достигающие 40-60% (Oda et al., 2006). Пятилетняя выживаемость раннего рака составляет более 90% (Tan and Fielding 2006). Японскую модель раннего обнаружения трудно воспроизвести в других популяциях. В группах населения с низким риском скрининг населения не является экономически эффективным. В развивающихся странах с высоким риском развития рака желудка экономические и материально-технические условия препятствуют принятию такой практики. Поэтому привлекательным предложением снизить заболеваемость и смертность от рака желудка является выявление субъектов с высоким риском, которые могут воспользоваться целевым скринингом и другими профилактическими мерами для предотвращения развития рака.
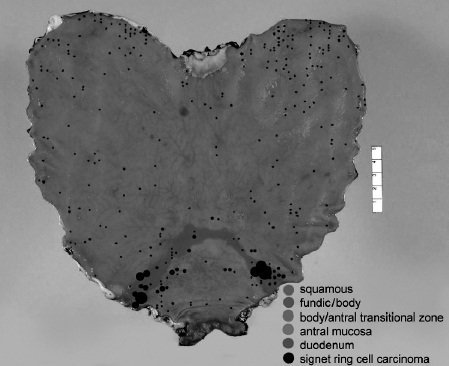
Гастрэктомический экземпляр 15-летней девочки-подростка маори с наследственной диффузной аденокарциномой. Каждый фокус карциномы in situ, обозначенный грубо, изображен черной точкой. В этом образце было выявлено 318 карцином in situ. Опухоли вокруг муравьиного соединения были больше. (Фотография любезно предоставлена доктором Амандой Чарлтон, Отделом патологии, больницей Мидмормор, Окленд, Новая Зеландия. Воспроизведена с Charlton et al., 2004, с разрешения.)
В настоящее время имеются данные о том, что полиморфные изменения в ряде генов могут помочь идентифицировать восприимчивых субъектов, тех носителей генетических ассоциированных с аллели аллелей и инфицированных вирулентными штаммами H. pylori. Исследование, проведенное в Португалии, показало, что субъекты, переносящие полиморфизм IL1B-511T и инфицированные cagApositive бактериями, имеют относительный риск в 25 раз больше, чем те, у которых нет аллеля T, инфицированного cagA-отрицательными бактериями. Для субъектов, несущих полиморфизм IL1B-511T, инфицированных H. pylori vacAs1, риск в 87 раз выше, чем у тех, у кого меньше вирулентных генотипов (vacAs2) и IL1B-511CC (Figueiredo et al., 2002). Теперь можно диагностировать состояние H.pylori, cagA и vacA с помощью серологических методов (Blaser et al., 1995; Camorlinga-Ponce et al., 1998; Ghose et al., 2007). Наличие нескольких связанных с риском аллелей может облегчить идентификацию субъектов с высоким риском.

Микрофотография слизистой оболочки желудка у португальского пациента с наследственной диффузной аденокарциномой. (A) Неопластические бокаловидные клетки видны у основания эпителия снегового и железистого. (B) Оксинтрическая слизистая оболочка, показывающая распространение пугалоидов злокачественных неопластических бокаловидных клеток (стрелки). (Фото предоставлено доктором Фатимой Карнейро, Институтом молекулярной патологии и иммунологии Университета Порту, Португалия).
Длительный предраковый процесс предлагает возможности для вмешательства, чтобы предотвратить его прогрессирование. Несколько исследований по химиопрофилактике сообщили, что эрадикация H.pylori предотвращает прогрессирование предраковых поражений (Fuccio et al., 2007). Имеющиеся данные свидетельствуют о том, что лечение инфекции в начале процесса, до развития атрофии и метаплазии, предотвращает рак желудка (Wong et al., 2004). Дополнительные данные из крупномасштабного ретроспективного многоцентрового исследования в Японии, проведенного у пациентов, перенесших верхнюю желудочно-кишечную эндоскопию, показали, что эрадикация H.pylori уменьшила частоту рака желудка (Kato et al., 2006b). Потому что в большинстве стран с высоким риском инфицировано более 70% субъектов, массовая анти-H. Пилори терапия нереальна и не подходит.

Таким образом, профилактика должна быть стратегией борьбы с раком желудка. Меры по профилактике заболеваний различаются по численности населения. Особое внимание следует уделить опухолям с семейной агрегацией и карманами высокого риска в странах с низким риском развития рака желудка. Идентификация лиц с наивысшим риском среди населения в целом может быть достигнута путем тестирования образцов крови на маркеры генетической восприимчивости, а также инфекции с очень вирулентными штаммами H. pylori. Выявленные субъекты должны вводить программы эпиднадзора на основе эндоскопического мониторинга, направленные на выявление и лечение дисплазий и ранних карцином.
Несколько мер общественного здравоохранения для снижения риска развития рака желудка должны включать лечение и ликвидацию гастрита H. pylori, снижение потребления соли и содействие адекватному потреблению свежих фруктов и овощей. Следует ожидать, что светская тенденция к снижению частоты рака желудка будет продолжаться. Такое устойчивое снижение может быть ускорено путем адаптации вышеупомянутых стратегий профилактики.