«Эпидемия фуфломицинов» — где так можно описать, то что происходит сейчас в медицине.
Количество назначений неэффективных лекарственных средств, целью которых является выкачивание денег, превышает любые разумные пределы, пациенты же тратят на них последние деньги.

И хотя об этой проблеме все чаще говорят и пытаются с ней бороться, но существенных результатов пока не видно.
Описывать возможные законодательные изменения для исправления ситуации не имеет смысла, потому что рецепт известен и нужна лишь политическая воля.
Поэтому предлагаю не дожидаясь политические решения попробовать разобраться в том, какие лекарства имеют доказанную эффективность, а какие нет.
Возможно, проще было бы написать несколько простых лайфхак, но использование их без понимания базовых вещей не поможет и быстро забудется, потому распишу все более детально.
Хочу сразу предупредить, что эта статья не является руководством по самолечению, но она должна научить задавать вопросы врачам, фармацевтам и другим специалистам от медицины.
Сначала попробуем разобраться с тем, как же лекарства становятся лекарствами, потому что без этого довольно тяжело говорить об оценке их эффективности.
Существует два основных подхода в создании лекарств.
- Первый — идет путем поиска заболевания, которое сможет лечить уже известна вещество (обычно это вещества, которые были выделены из растений, бактерий или других организмов).
- Второй — идет путем нахождения вещества, будет лечить конкретное заболевание (искусственно синтезированные вещества).
На сегодня большинство лекарств разрабатываются по другому пути, но не стоит отбрасывать и первый, потому что он уже позволил найти много эффективных лекарств.
Например, такое вещество как рапамицин была выделена из бактерии Streptomyces hygroscopicus, которая была найдена в образцах почвы с острова Пасхи. И только после лет исследований у нее было обнаружено иммуносупрессивную действие, вследствие ингибирования протеинкиназы mTOR. И теперь рапамицин применяется для профилактики отторжения органов после трансплантации. И не факт, что эта молекула когда-то была бы создана человеком.
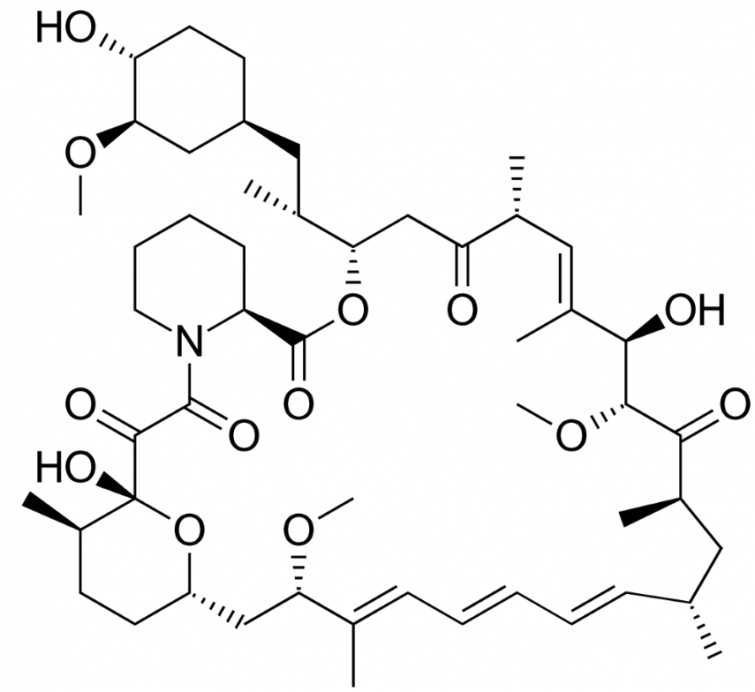
Рапамицин или cиролимус
С другой стороны, человек создал вещества, не существуют в природе, например, инфликсимаб — причудливое моноклональное антитело (генетический код полученных антител является комбинацией ДНК мыши и человека), которое избирательно связывается с цитокинов ФНО-α.
Этот препарат сейчас применяется для лечения болезни Крона, псориаза и ряда других заболеваний, а за открытие принципа создания такого типа веществ в 1984 году Сезар Мильштейн, Георг Кёлер, Ерне получили Нобелевскую премию.
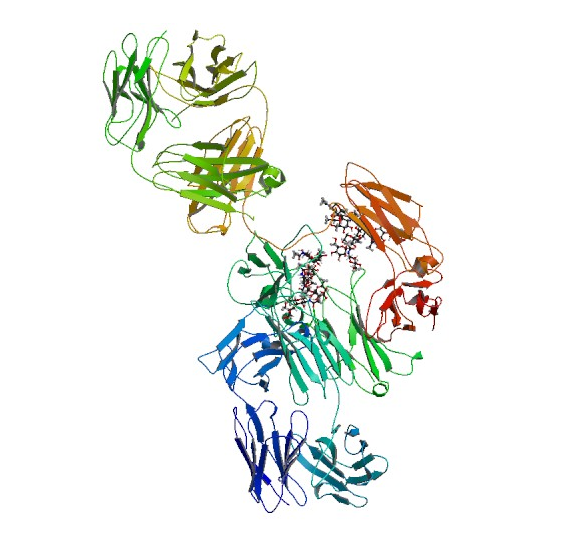
Инфликсимаб
Но мы вернемся к процессу разработки лекарств. Фармацевтические компании, принимая решение о разработке лекарственных средств, отталкиваются от имеющейся научной экспертизы и бизнес составляющей. После того, как менеджмент выбирает определенное заболевание, ученые исследуют имеющуюся информацию о заболеваниях и начинают поиск биологических мишеней, воздействие на которые, по их мнению, позволит корректировать заболевания (это могут быть белки, ферменты, ионные каналы и т.д.).
В настоящее время существует более 1400 утвержденных в США и ЕС действующих веществ, но взаимодействуют они только с 324 мишенями .
Любой препарат, имеет мишень или несколько мишеней, с которыми он взаимодействует. Сейчас уже известны основные мишени и механизмы действия многих лекарственных средств, которые были открыты человечеством в прошлом.
Лекарственное средство не может просто так взять и снизить давление, но он может подавить действие АПФ, который в свою очередь будет меньше превращать ангиотензин I в ангиотензин II, и таким образом уменьшится его сосудосуживающее действие и произойдет расширение сосудов, что приведет к снижению давления — и это является механизмом действия ингибиторов АПФ (такие препараты как, эналаприл, лизиноприл, рамиприл).
Таким образом, если в препарата нет мишени и механизма действия — его эффективность сомнительна, а некоторые исключения лишь подтверждают общее правило.
После того, как ученые выбрали потенциальную мишень, на которую они хотят влиять, необходимо найти вещества, которые могут это сделать. Для этого разрабатываются специальные банки химических веществ, содержащих миллионы молекул.
Молекулы сначала тестируют с помощью компьютерного моделирования, а уже потом перспективные молекулы проверяются на специальных биохимических и клеточных моделях с применением различных методик (радиологических, электрофизических, иммуноферментных, генетических и других) и таким образом определяются те молекулы, должны влиять на мишени.
После этого значительно меньшее количество отобранных веществ тестируют уже на специально разработанных животных моделях, которые позволяют как можно точнее имитировать заболевания, ведь течение заболеваний у людей и животных разный или вообще животные не болеют человеческими болезнями.
Например, для моделирования муковисцидоза была создана специальная генетически модифицированная линия свиней, а для исследования гипертонической болезни — линия спонтанно гипертензивных крыс.
Ранее же исследования проводились на обычных домашних мышах, пока в 1906 году в Wistar Institute не была создана первая стандартизированная линия крыс Wistar, и сейчас более 50% лабораторных крыс является их потомками.

Трансгенные мыши, экспрессирующие ген усиленного зеленого флуоресцентного белка (eGFP).
После проведения доклинических исследований на менее двух видах животных и получения положительных результатов относительно эффективности и безопасности начинается этап исследования на людях — клинические исследования.
Прежде документально засвидетельствовано клиническое испытание было проведено в 1747 году, шотландским врачом Джеймсом Линдт , который при поиске средства для лечения и предупреждения цинги (недостаток витамина С) разделов 12 моряков с симптомами цинги на 6 групп и дал им следующие вещества: сидр, разведенную серную кислоту, уксус, морскую воду, смесь нескольких продуктов (в том числе мускатного ореха и чеснока) и апельсины с лимоном.
Уже через неделю морякам, получавших цитрусовые стало значительно лучше. Таким образом, так и не узнав причины цинги, он нашел эффективный способ ее лечения.
Современные клинические исследования начинаются сначала на нескольких десятках здоровых добровольцев, получающих за это деньги (на других фазах участие бесплатное), и на которых проверяют безопасность препарата, дозировка и некоторые другие фармакологические показатели.
В случае подтверждения безопасности переходят к фазе 2 клинических исследований, когда происходит ограниченное исследования эффективности и побочных эффектов на нескольких сотнях больных.
После этого производители переходят к фазе 3 клинических исследований, когда привлекается уже большое количество пациентов, может достигать нескольких тысяч.
Такие исследования проводятся сразу во многих странах. По данным портала clinicaltrials.gov в 2016 году в США началось более 8161 клинических исследований различных фаз.
«Золотым стандартом» для современных исследований является рандомизированные, вдвойне-слепые, плацебо-контролируемые исследования — это значит, что существует как минимум две группы сравнения (плацебо или обычная терапия и экспериментальное лечение), в одну из которых пациент попадает случайно и никто не знает, в которую из этих групп он попал.
Это позволяет устранить субъективные и / или бессознательные предубеждения участников исследования.
Впервые такое исследование было проведено в 1948 году во время испытания эффективности лечения стрептомицином больных туберкулезом.
Современные стандарты для исследований возникли не сразу.
Одним из крупнейших вызовов для клинических исследований является исследование безопасности. К 1937 году не существовало установок и требований для исследования безопасности лекарственных средств.
Первые изменения были обусловлены трагедией, произошедшей из-за того, что к средству для лечения стрептококковой инфекции Elixir sulfanilamide добавили диэтиленгликоль и это повлекло 107 смертей в США.
В 1961 году произошла талидомидова трагедия, когда из-за снотворное средство родилось более 10000 детей с уродствами конечностей. Причиной же было то, что ученые ошибочно считали, что плацентарный барьер между матерью и ребенком обеспечивает достаточную защиту и не пропускает химические вещества и поэтому исследование безопасности для плода на животных не проводились.
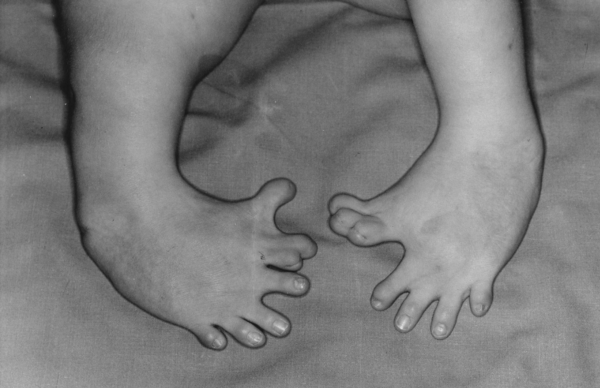
Дефект ступни из-за применения талидомида.
Кроме этого был еще ряд других трагедий и каждая из них предопределяла усиления и совершенствования регуляторных требований к безопасности и эффективности лекарственных средств.
В случае успешного завершения нескольких клинических исследований фазы 3, фармацевтические производители подают документы на рассмотрение в регуляторных органов, в Европе это European Medicines Agency, в США это Food and Drug Administration (отдел, занимающийся вопросом регистрации новых лекарств и имеет бюджет более 290 млн долларов США).
Общий же научно-исследовательский бюджет фармацевтических производителей составил более 154 млрд долларов США в 2016 году без учета расходов на фундаментальные исследования, финансируемые из других источников. Такие расходы позволяют ежегодно регистрировать около 50 новых лекарственных средств в США и ЕС, а стоимость разработки нового лекарственного препарата составляет более 2 млрд долларов США.
Стоит отметить, что новые лекарственные средства получают патентную защиту, продолжительность которого зависит от страны и других условий, но в среднем составляет 20 лет.
Именно за это время производители могут вернуть вложенные инвестиции и заработать. По истечении этого срока, все остальные фармацевтические производители также получают право производить лекарства с тем же действующим веществом, такие лекарства называются дженериками.
Надеюсь, теперь вы понимаете, насколько сложный процесс создания инновационного лекарственного средства с доказанной эффективностью и безопасностью. И поэтому когда, кто-то говорит, что возможно «в гараже» разработать панацею, то это заставляет задуматься ли мошенник или дурак перед вами.
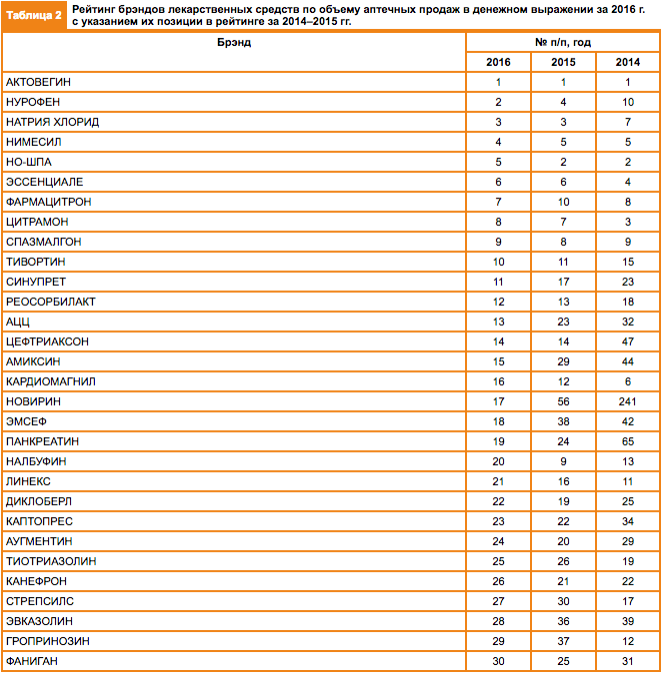
ТОП-30 лекарственных средств по данным газеты
Почему же сомнительные лекарственные средства настолько популярны?
Причины этого могут быть разные.
Во-первых, фармацевтические производители могут платить врачам за лояльность к их препаратов материальными или другими благами.
Для того, чтобы понять масштабы этого явления, надо честно признать, что когда консультация врача бесплатная или стоит «коробку конфет», то заинтересовать врачей назначать те или иные лекарства очень просто.
Во-вторых, низкое качество базового и последипломного медицинского образования делает врачей чрезвычайно «уязвимыми» перед многотысячной армией медицинских представителей, каждый день пытаются убедить 186000 врачей в эффективности их препаратов.
Кроме этого, наши врачи почти не читают англоязычную литературу, в то время, когда большинство отечественной является «джинсой». Поэтому сложилась ситуация, когда медицинскую информацию врачи получают не из независимых источников, а исключительно от фармацевтических компаний.
В-третьих, неистовый недостаток доверия к врачам стимулирует пациентов к самолечению с помощью интернета и советов работников аптек, должны выполнить план продаж. Дополнительно свое дело делает и телевизионная реклама.
В общем причиной этой ситуации является институциональная слабость, в развитых странах между врачом и пациентом всегда есть посредник, который платит лечения и контролирует расходы.
Это могут быть страховые компании или другие институты, руководствуются определенными стандартами лечения.
Большую часть лекарств пациенты покупают за деньги, и поэтому не имея специальных знаний, они вынуждены доверять врачам.
Попробуем разобраться в том, из каких источников можно получить максимально объективную информацию об эффективности лекарств.
Каждый препарат, который продается в аптеке имеет два названия — торговое наименование (бренд), которое дает производитель и международное непатентованное наименование (МНН), что характеризую действующее вещество.
Общее количество МНН сейчас составляет примерно 7000 наименований и растет с каждым годом. Поэтому если лекарственное средство не имеет МНН, то сразу вызывают большие сомнения в целесообразности его применения.
Надо отметить, что МНН не предоставляется растительным, гомеопатическим препаратам, химическим соединениям (например, acetic acid) и лекарствам, давно используются и хорошо известны под собственными названиями (например, morphine, codeine).
Теперь перейдем к самому интересному.
Давайте проанализируем известные действующие вещества, например, amitriptyline в лечении больных с депрессией и Умифеновир (ранее известный под одной из торговых названий как «Арбидол») для лечения больных гриппом.
1. Как вы узнали выше, жесткая система оценки эффективности и безопасности лекарств в США и ЕС.
Поэтому сначала узнаем зарегистрированы там указаны лекарственные средства. Для этого можно выполнить поиск на сайтах регуляторных органов FDA и EMA , или же просто зайти на сайт-агрегатор www.drugbank.ca и выполнить поиск там.
Как можно увидеть амитриптилин имеет профиль на сайте DrugBank и отметку «approved», что означает, что он разрешен к применению в США и / или ЕС.
В свою очередь лекарственные средства, содержащие умифеновир запрещены к применению в США и ЕС.

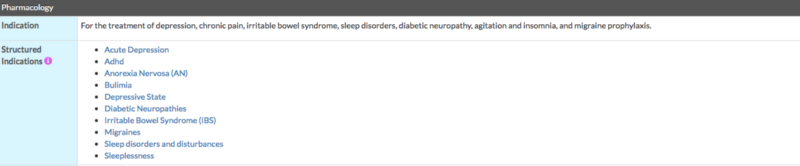
2. Попробуем разобраться в правильности назначения этих средств. Для этого на том же сайте DrugBank можно найти в разделе «structured indication», что переводится как «показания к применению» и там будет указано, что амитриптилин назначается при различных психиатрических заболеваниях в том числе и при депрессии.
Также по ключевым словам «amitriptyline, fda, label» можно найти инструкции к применению в США и ознакомиться с ней.
В связи с тем, что лекарственные средства, содержащие umifenovir не зарегистрированы в США / ЕС, мы не можем воспользоваться таким поиском и должны (или не должны) доверять регуляторам СНГ.
3. Кроме этого важна количество научных публикаций, поскольку научный интерес к фармакологической вещества хоть и не прямым, но косвенным свидетельством эффективности.
Ведь очевидно, что ученые и врачи не будут исследовать лекарственные средства, которые являются не эффективными.
Для проверки этого параметра можно воспользоваться наукометрическими базой PubMed, которая содержит более 8747 статей с упоминанием «Amitriptyline», другая же база Google Scholar содержит 118000 упоминание амитриптилин.
В то же время, по поиску «umifenovir» PubMed дает 116 публикаций, а Google Scholar — 91.
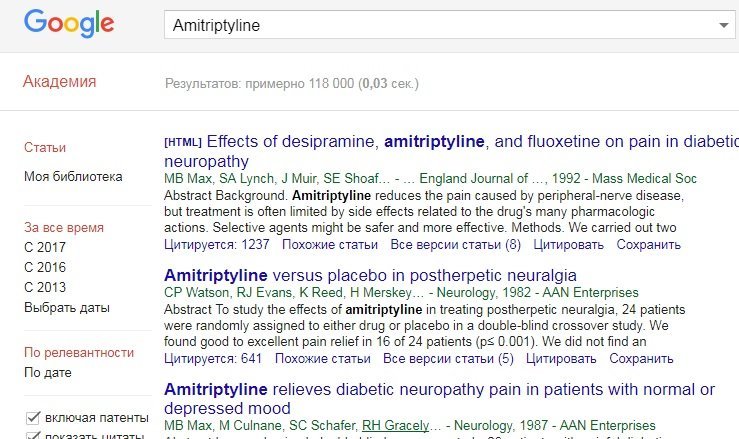
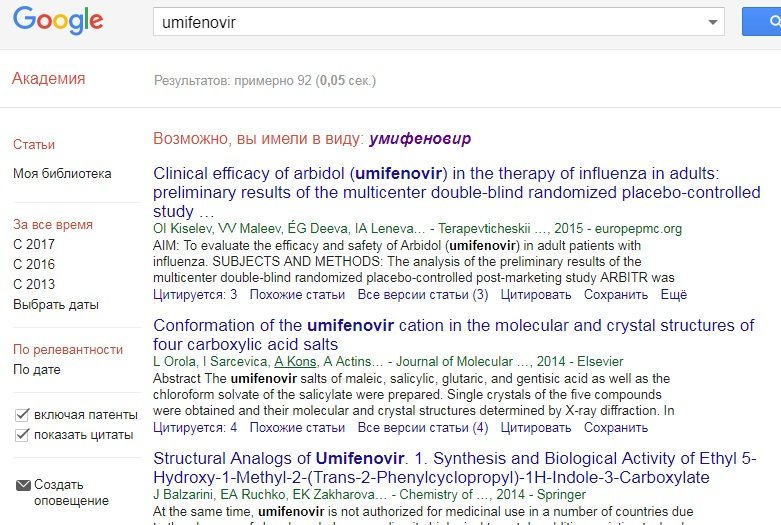
Также необходимо обратить внимание на то, что статьи о амитриптилине пользователя многонациональными коллективами ученых, опубликованные в авторитетных рецензируемых журналах и активно цитируются другими учеными.
О умифеновире такое сказать нельзя.
4. Попробуем разобраться с клиническими исследованиями.
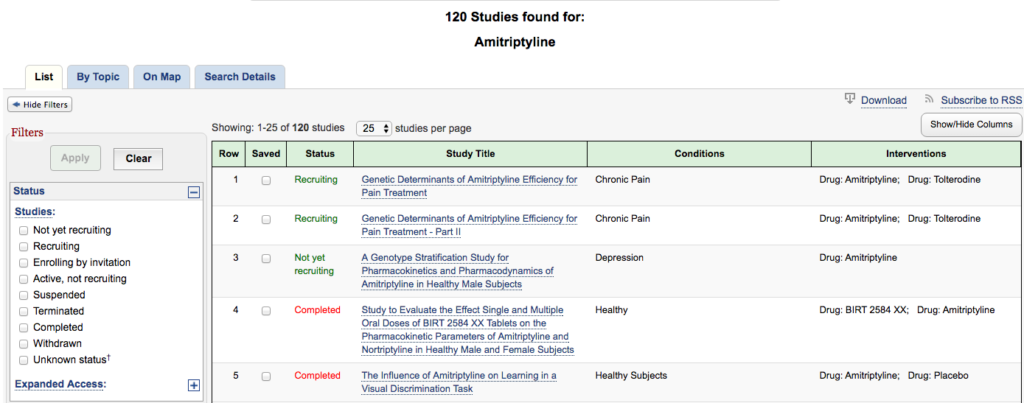
С помощью сайта www.clinicaltrials.gov, на котором размещаются информация о международных клинические исследования можно узнать о 120 клинических исследования амитриптилина. И очевидно, если бы амитриптилин был не эффективен или опасен, то исследования остановились бы после нескольких неудач.
Но мы видим, что исследования продолжаются и ученые ищут новые показания к применению.
В то же время было проведено только 1 исследование умифеновиру, о чем это свидетельствует я думаю вы понимаете.
5. Кроме этого можно обратиться к Всемирной организации здравоохранения, которая разрабатывает Ориентировочный перечень жизненно необходимых лекарственных средств , содержащий лекарства с доказанной эффективностью и безопасностью, но дополнительно еще с учетом целесообразности расходов для удовлетворения наиболее важных потребностей в системе здравоохранения.
Поэтому в этот перечень могут не попасть эффективные и дорогостоящие лекарства.
Если их открыть, то можно узнать, что амитриптилин содержится и в Перечне ВОЗ и в Национальном перечне, а умифеновир — нет.
6. Кроме того, чтобы не потеряться в обилии информации существуют систематические обзоры (review) — работы по осмотру ряда опубликованных отдельных однородных оригинальных исследований с целью их критического анализа и оценки.
Одним из самых авторитетных источников таких осмотров является Кокрановское Сотрудничество , изучающая эффективность медицинских средств и методик.
Одним из обзоров касается лечения депрессии амитриптилином и общий вывод авторов заключается в том, что он является эффективным в лечении депрессии, но имеет больше побочных эффектов чем некоторые другие антидепрессанты.

Вот что говорит один из самых авторитетных источников обзоров эффективности препарата — Кокрановское Сотрудничество
Результатов Кокрановского Сотрудничества учитывая эффективности лечения умифеновиром гриппа не было на момент публикации.
Подытоживая отмечу, что однозначно говорить об эффективности лекарственного средства или его отсутствие невозможно. Однако каждая организация или человек могут изучить имеющуюся информацию и сделать для себя выводы.
Надеюсь, что информация поможет вам разобраться в эффективности и безопасности лекарств, которые вы или ваши родственники и друзья принимают.
В то же, время необходимо понимать, что 15-минутная статья не сделает из вас врача, поэтому используйте эти знания для того, чтобы задавать вопросы, а не заниматься самолечением.
Хочу отметить, что лично мне было бы довольно трудно ответить на вопрос «А почему вы мне назначили препарат Х, который не применяется в США / ЕС, не рекомендуется ВОЗ, и не имеет международных клинических исследований?»