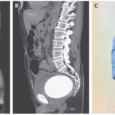
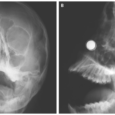
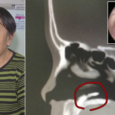
Под неонатальным волчанкой (НВ) понимают симптомокомплекс, который диагностируют у новорожденных, матери которых страдают системным заболеванием соединительной ткани (СЗСТ) с наличием антител (АТ) к антигенам Ro (SS-A) и La (SS-B), и чаще всего проявляется двум признакам — поражением кожи и проводящей системы сердца. НВ случается с частотой 1 на 15-20 тыс. новорожденных и чаще среди белого населения планеты. Проблема своевременной диагностики и прежде всего в том, что предотвращение НВ тесно связано с повышением качества оказания медицинской помощи женщинам с аутоиммунными заболеваниями и позитивными изменениями в вопросах планирования беременности у таких женщин.
Из истории изучения
В 1954 году CH McCuistion и EP Schoch впервые описали типичные кожные проявления у ребенка, мать которого страдала системной красной волчанкой (СКВ), и предложили термин «neonatal lupus erythematosus», что надолго закрепило этот не совсем точный термин в мировой литературе. Позже, в 1983 году, JS Scott, PJ Maddison и соавт. впервые предположили наличие взаимосвязи между материнскими АО к рибонуклеопротеидам и врожденной блокадой сердца (ВБС) у новорожденных. Сейчас в Международной классификации болезней 10-го пересмотра (МКБ-10) НВ содержится в рубрике Р.83 ( «Другие изменения наружных покровов, специфичные для плода и новорожденного»), в англоязычной литературе используются как синонимы термины «neonatal lupus syndrome», «congenital lupus», «congenital lupus erythematosus», «neonatal lupus erythematosus», из которых, по нашему мнению, ближайшим к сущностной характеристики этого синдрома является первый.
Клинические проявления
По данным мировых литературных источников, подавляющее большинство случаев НВ проявляется в виде изолированных форм, среди которых чаще всего встречаются кожные высыпания (25-32% в общей картине) и поражения сердца (15-24%). Кожная сыпь обычно представлена полициклическими сливными элементами, которые локализуются на коже головы, шеи и верхних конечностей, появляются в течение первых 6-8 недель жизни и нередко усиливаются на фоне инсоляции. Что касается поражения сердца, то оно включает миокардит с нарушениями сердечного ритма и проводимости (блокада 1, 2 степени); полную поперечную блокаду сердца с сочетанием или без клапанных пороков (в 15-20% случаев приводят к гибели плода) дилатационная кардиомиопатия, ендокардиофиброеластоз тому подобное. Проявления со стороны других систем и органов, такие как тромбоцитопения, анемия, гепатомегалия, транзиторная гипербилирубинемия, спленомегалия, пневмонит, составляют около 15-18% случаев и обычно преходящий характер. В 30-40% случаев НВ манифестирует сочетанием различных клинико-лабораторных проявлений. Наличие в анамнезе ребенка НВ не является предпосылкой развития аутоиммунного заболевания в подростковом или взрослом возрасте, хотя в литературе описаны случаи развития СКВ или болезни Шегрена у таких детей.
Считается, что именно АТ к Ro (SS-A) и La (SS-B) принадлежит ведущая роль в патогенезе НВ, при этом развитие кожных проявлений связывают прежде всего с АО в La (SS-B), а ВБС — с наличием АТ к Ro (SS-A). Последние представлены белками с молекулярной массой 52 и 60 кДа, из которых более патогенными являются полипептиды массой 52 кДа. E. Jaeggi, C. Laskin и соавт. в своем исследовании показали наличие корреляции между титрами АТ к Ro (SS-A) и развитием ВБС и отметили, что клинически значимым является титр АТ ≥50 Ед / мл.
Матери новорожденных с НВ. АТ к Ro (SS-A) и La (SS-B) выявляются при таких аутоиммунных заболеваниях, как СКВ с синдромом Шегрена или (реже) без него, дискоидная красная волчанка, что ассоциируется с наличием АТ к La (SS-B), болезнь Шегрена (первичный синдром Шегрена), системная склеродермия с синдромом Шегрена, ревматоидный артрит с синдромом Шегрена, другие аутоиммунные заболевания (первичный билиарный цирроз печени, аутоиммунный тиреоидит) с синдромом Шегрена.
Следует отметить, что не у всех матерей, имеющих АТ к Ro (SS-A) и La (SS-B), рождаются дети с НВ: всего лишь в 2-5% новорожденных диагностируют это заболевание, в 1-3% случаев развивается ВБС. Это позволяет предположить, что, кроме материнских АО, есть и другие факторы, которые обусловливают развитие НВ. Установлено, что риск рождения больного ребенка повышается при наличии HLA-B8 и HLA-DR3. Вероятно, определенную роль играют половые гормоны: соотношение больных девочек к мальчикам составляет 2: 1, что связывают с усилительные эффектом эстрадиола. Интересно, что риск рождения второго ребенка с ВБС у больной матери растет в 6-10 раз, даже если первый ребенок имела только кожные проявления, ассоциированные с материнскими АО к Ro (SS-A) и La (SS-B). Кожная форма встречается чаще у детей, матери которых не имели диагностированного СЗСТ. По разным данным, у 70-90% матерей, которые не имели СЗСТ на момент рождения больного ребенка, в течение десяти лет развивается аутоиммунное ревматическое заболевание.
Лечение и профилактика
Сейчас протокола лечения НВ не разработано, но с учетом результатов последних исследований сформулированы рекомендации по предотвращению развития и лечения этого синдрома. Они содержат следующие пункты:
- Больным женщинам с установленным диагнозом рекомендуется принимать профилактические дозы гидроксихлорохина за 6 недель до планируемой беременности и все время в течение беременности. Эффективность применения высоких доз дексаметазона, плазмафереза и внутривенного введения иммуноглобулина не было доказано.
- Начиная с 16-й недели беременности обеспечить еженедельную допплерометрию сосудов пуповины для своевременной диагностики задержки внутриутробного развития и эхокардиографическом (ЭхоКГ) исследования для мониторинга развития сердца плода, ведь манифестация кардиальных осложнений обычно наступает с 18-го по 24-ю неделю гестации, что повязкам связано с повышением трансплацентарного транспортировки IgG во II триместре.
- Роды должны быть запланированы в учреждениях третичного уровня для своевременного установления электрокардиостимулятора при ВБС.
- В случае диагностирования изолированной кожной формы, гематологических проявлений или отдельных проявлений со стороны других органов и систем ребенок лечения не требует.
- Ребенка наблюдать до 6-7 мес (в отдельных случаях — до 9) с контрольным анализом крови для подтверждения элиминации материнских АО.
Случай из клинической практики
Приведем клинический случай неонатальной волчанки у 3-месячной девочки, мать которой обратилась в клинику в августе 2016 с жалобами на сыпь на лице ребенка (фото).
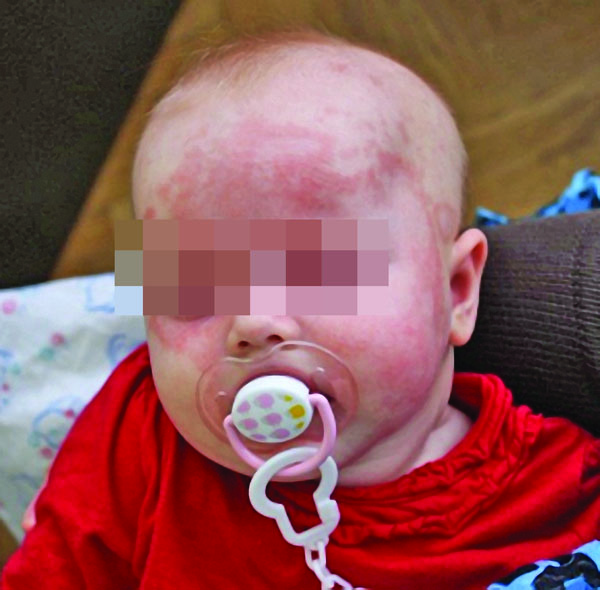
Анамнез ребенка: родился здоровым, но в возрасте 6 недель было замечено появление ярко-розового пятна в височной области слева, которая постепенно увеличивалась, стала кольцеобразной, со временем на лице появились новые пятнисто-кольцеобразные элементы с тенденцией к слиянию, увеличение. Повышение температуры, ухудшение общего состояния девочки не наблюдали, укусов клещей и насекомых не зафиксировано. Мать ребенка отметила, что под воздействием солнечных лучей сыпь становится более яркой. В связи с прогрессированием сыпи ребенок был госпитализирован в стационарную педиатрическую учреждение, где по результатам осмотров специалистов, общеклинических лабораторных исследований установлен диагноз токсикоалергичних дерматита. В результате лечения дексаметазоном наблюдалась положительная динамика: значительное уменьшение интенсивности экзантемой, однако после отмены препарата сыпь возобновилась.
У матери на момент обследования жалобы отсутствуют. Из анамнеза: беременностей — 3, родов — 2, имеет здорового сына 8 лет, вторая беременность — выкидыш. Два года назад перенесла «паротит» — наблюдалось припухлость околоушных слюнных желез, преимущественно левой, без признаков инфекционного заболевания. Лечение не получала, припухлость желез регрессировали за 2 нед. Во время целенаправленного опроса не получено информации о наличии жалоб или симптомов «ревматологического круга», включая артралгии, кожную сыпь, гипертермию, сухость во рту и глазах, однако женщина отметила, что во время длительной работы за компьютером или чтения появляется чувство «песка в глазах», чаще возникает желание моргнуть. На компьютерной томограмме челюстно-лицевой области, которую выполняли за 3 мес до обращения, зафиксировано увеличение поднижнечелюстных лимфатических узлов слева.
При осмотре матери клинически значимых отклонений со стороны доступных для физикального обследования органов и систем не найдены. В результатах предназначенных лабораторных и инструментальных исследований выявлен ряд диагностически значимых изменений: скорость оседания эритроцитов (СОЭ) — 42 мм / ч (референтные значения — до 20 мм / ч); С-реактивный белок (СРБ) — 34 мг / л (референтные значения — до 5 мг / л); ревматоидный фактор — 72 МЕ / мл (референтные значения — до 14 МЕ / мл) антинуклеарные антитела (АНА) — положительные (норма — отрицательные) АТ к Ro (SS-A) 52/60 и La (SS-B)> 8 Ед (отрицательный результат — до 1 Ед), другие АТ к ядерным антигенам — отрицательный результат; тимоловая проба — 14 Ед / л (референтные значения — до 4 Ед / л). Проба Ширмера показала существенное уменьшение продукции слезной жидкости с обеих сторон: ОD — 5 мм, OS — 7 мм (норма — не менее 15 мм за 5 мин). Рентгенография органов грудной клетки, электрокардиография (ЭКГ) и ЭхоКГ патологии не обнаружили.
Учитывая данные анамнеза (неассоциированный с инфекцией эпизод припухлость околоушных слюнных желез во взрослом возрасте, увеличение поднижнечелюстных лимфатических узлов, косвенные признаки снижения слезопродукции), лабораторных обследований (признаки активного воспалительного процесса — повышение СОЭ и уровня СРБ, высокий уровень ревматоидного фактора без признаков артрита, положительные АНА, значительное повышение АД до Ro (SS-A) и La (SS-B), тимоловой пробы при отсутствии отклонений в других печеночных тестах), подтвержденное с помощью пробы Ширмера двустороннее снижение п родукции слезной жидкости, матери был установлен диагноз: болезнь Шегрена, хроническое течение, 2 степень активности, с поражением слюнных (сиалоаденит, лимфаденопатия) и слезных желез (ксерофтальмия). АНА (+), АТ-Ro (SS-A) (+), АО-La (SS-B) (+), РФ (+). Рекомендовано провести ультразвуковое исследование слюнных желез и биопсию мелких слюнных желез слизистой оболочки рта.
После получения результатов обследования матери было принято решение дообследовании ребенка. В клиническом анализе крови — все показатели в пределах возрастной нормы, уровень СРБ не повышен, обнаружено АНА (положительные) и АО к Ro (SS-A) 52/60 и La (SS-B)> 8 Ед / л, другие лабораторные параметры, включая РФ и тимоловой пробы — без патологических изменений. Результаты ЭКГ и ЭхоКГ ребенка нормальные.
Учитывая наличие у матери болезни Шегрена с высокими титрами АТ к Ro (SS-A) и La (SS-B), обнаружение в крови девочки таких же АО при отсутствии клинико-лабораторных признаков СЗСТ ребенку установлен диагноз: неонатальный волчаночный синдром с поражением кожи (эритематозные дерматит). АНА (+), АТ-Ro (SS-A) (+), АО-La (SS-B) (+).
Итак, можно сделать вывод, что развитие НВ у этого ребенка было обусловлено трансплацентарной передачей материнских АТ к Ro (SS-A) и La (SS-B). Клиническая картина будет присутствовать до тех пор, пока не элиминируются материнские АО — ориентировочно в течение 3-4 мес, поэтому было рекомендовано наблюдать ребенка до 6-месячного возраста и ожидать уменьшения сыпи до полного ее исчезновения. Системное лечение в этом случае показано, стоит лишь избегать попадания на кожу ребенка прямых солнечных лучей, что может спровоцировать появление новых высыпаний или усилить их выраженность. Возможно местное применение глюкокортикоидных кремов или мазей. Матери было рекомендовано после дообследования наблюдаться у ревматолога для лечения заболевания в будущем, согласовывая его инициацию с окончанием грудного вскармливания. Хотя, согласно современным рекомендациям Европейской противоревматической лиги (EULAR) с фармакотерапии ревматических заболеваний во время беременности и лактации, женщина может без вреда для ребенка принимать глюкокортикоиды и некоторые другие лекарственные средства, относительно доброкачественное течение заболевания у матери позволяет на несколько месяцев отложить начало лечения.